 |
北京2017年5月4日電 /美通社/ -- 創建於中國-新加坡蘇州工業園區生物納米園(Suzhou-SIP Biobay)、致力於具全球自主知識產權的創新單抗藥物研究與產業化的生物製藥企業蘇州思坦維生物技術有限責任公司(簡稱思坦維或Stainwei)日前獲悉:該公司已進入臨床研究階段、全新的抗腫瘤血管增生(抗VEGF)單抗藥物(代號hPV19)日前已正式獲得美國專利商標局(USPTO)頒發的專利授權證書(專利號:US9,580,498),該專利的有效期截至2032年。這也是公司該單抗繼2015年、2016年先後獲中國國家知識產權局頒發兩項專利授權證書之後,在單抗藥物領域全球專利申請與戰略佈局中取得的又一重要里程碑事件。
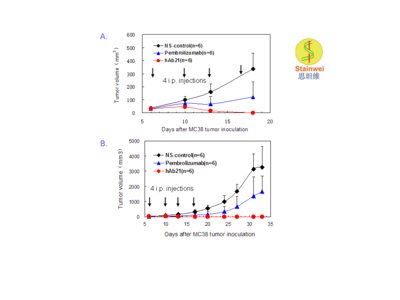
抗PD-1 單抗hAb21在PD-1人源化小鼠移植腫瘤模型中測試結果 PD-1基因人源化純合子小鼠(基因背景為C57BL/6) 背部皮下接種數量約為1 x106的同源的小鼠結腸癌細胞MC38,待接種的腫瘤體積長至米粒大小時(約50mm3,接種後第6天),將動物隨機分為3組(每組6只),分別在接種後第6, 10, 13及 17 天腹腔注射200 ug抗PD-1單抗pembrolizumab, hAb21 單抗或生理鹽水。其中圖A為接種腫瘤的生長早期曲線; 圖B為接種腫瘤的生長全程曲線。
思坦維在研的VEGF單抗不但具有全新的氨基酸序列及獨特的抗原識別位點(epitope), 且體內外生物活性比全球首個也是目前唯一獲美國FDA批准上市的VEGF單抗藥物Avastin (商標名:Beavacizmab Roche/Genentech公司的重磅炸彈級產品,2015年全球年銷售額67億美元)強6-8倍。 據公司負責人及該專利主要發明者之一周群敏博士介紹:「在臨床前動物研究及目前在腫瘤患者中開展的I期臨床研究中,hPV19單抗表現有很好的安全性/耐受性與初步療效。」 周群敏博士還表示:「憑其獨特的抗原識別表位、良好的安全性/耐受性及優於同類已上市藥物(Avastin)的生物活性, hPV19 單抗藥物如今後最終通過臨床研究成功開發上市,其意義不但可為國內外眾多腫瘤患者提供新一代的抗腫瘤血管增生藥物;未來臨床上還有望用於Avastin或其生物仿製藥治療無效或產生耐藥的患者,進一步開拓抗血管增生藥物的適應症與國內外市場。」
思坦維公司在hPV19單抗基礎上還開發出一眼用生物製品新劑型藥物,擬用於治療老年黃斑變性(age-related macular degeneration,AMD)及糖尿病性黃斑水腫等與血管增生/滲透相關的致盲性眼底病,目前該項目已申請專利,臨床前各項研究已完成,在申報臨床批件中。
除抗血管增生VEGF單抗藥物之外, 思坦維公司目前在研的另一重大項目是以通過調動機體自身免疫功能來直接攻擊或殺滅腫瘤為目的抗PD-1單抗藥物。思坦維公司已成功獲得一代號為hAb21、全新的抗人PD-1單抗(人源化IgG4-kappa 型)。hAb21單抗結合PD-1抗原的區域/結合位點(epitope)既不同於美國Merck公司已上市的Keytruda (通用名:Pembrolizumab),也不同於美國Bristol-Myers Squibb 公司已上市的Opdivo(通用名:Nivolumab)。 更驚奇的及更具臨床價值與產業化意義的是思坦維公司的hAb21單抗在PD-1人源化小鼠測試中,其抗腫瘤效果遠好於同類藥物Pembrolizumab。如圖所示,所有接受了hAb21單抗治療的動物在給藥7-10天後,腫瘤全部出現萎縮或徹底消失,在完成第4次給藥(也是最後一次給藥)後停藥30天以上,腫瘤也無恢復生長;而6只接受了Pembrolizumab治療的小鼠,僅有1只(16%)動物腫瘤出現萎縮或徹底消失;其餘5只在停藥後7-10天,腫瘤大多又都恢復生長並很快導致動物死亡或安樂死。先前接受過hAb21單抗治療的小鼠在第30天再重新接種MC38腫瘤 (無進一步給藥),腫瘤相繼在接種後10-14天內又都被徹底排斥;這批小鼠目前已第三次接種MC38腫瘤,各測試動物都依然健康存活(研究還在繼續進行與觀察中)。
基於這些令人鼓舞的結果,思坦維已經提交了有關hAb21單抗的專利保護申請,目前正圍繞臨床批件的申報在開展各項研究,計劃將在2017年底向中國CFDA及美國FDA提交資料申報臨床批件。
關於Stainwei Biotech, Inc.
蘇州思坦維生物技術有限責任公司 (www.stainwei.cn) 2007年成立於蘇州,致力於具全球自主知識產權的創新單抗藥物研究與產業化。公司目前在研主要產品線包括已進入臨床研究階段的廣譜治療多種腫瘤的VEGF單抗及在申報臨床批件階段的治療老年黃斑變性(AMD)等疾病的眼用抗VEGF單抗藥物劑型及抗腫瘤的PD-1單抗藥物。 此外,還有針對PD-1H(VISTA)、CTLA-4、SOST及其他多個全球創新靶點(first-in-class)等近10個創新單抗藥物在研。
公司自成立以來,先後獲得蘇州凱風創投、蘇州香塘創投、上海東方匯富、安徽同華創投等多家專業 VC/PE機構及多位自然人投資與支持。公司在研的VEGF單抗藥物項目還分別獲得國家十二五「重大新藥創製」重大新藥專項資金、江蘇省、蘇州市及中國-新加波蘇州工業園區等各級政府的科技資金資助。
思坦維公司聯繫方式: BD@stainwei.cn
圖片 - https://photos.prnasia.com/prnh/20170502/1836482-1
圖標 - https://photos.prnasia.com/prnh/20170503/1836482-1-a
精選視頻

- 简体中文 |
- English |
- 日本語 |
- 한국어 |
- Bahasa Indonesia |
- Tiếng Việt




