香港2020年8月17日 /美通社/ -- 中國領先的生物製藥公司三生製藥(01530.HK)今天公佈2020年上半年業績:儘管受全球新冠肺炎疫情影響,公司各項業務依然保持穩健增長態勢,並加速推進研發管線。未來,公司將繼續力克時艱,砥礪前行,發揮研發、生產、銷售、投資合作為一體的體系化競爭優勢,引領民族生物製藥產業長足發展,為患者和社會創造更大價值。
保持持續盈利能力
2020年上半年,三生製藥在疫情緩解後有序復工,共實現營業收入人民幣約26.95億元,比去年同期增長2.0%;毛利約人民幣22.17億元,比去年同期增長1.5%;歸母淨利潤人民幣約7.03億元,同比增長118.6%;正常化EBITDA約10.49億元,比去年同期增長3.1%;槓桿比率(不含債券)由2019年同期的13.7%下降至4.1%。
憑借成熟商業化團隊護航,三生製藥核心產品保持收入穩定。根據IQVIA數據,用於治療血小板減少症的特比澳在2020上半年銷售額13.75億元,同比增長15.2%,市場份額增至72.8%;用於治療類風濕性關節炎、強直性脊柱炎及銀屑病的益賽普銷售額3.31億元,市場份額54.5%;這兩種產品仍處於產品生命週期的早期階段,在中國的滲透率較低,臨床需求遠未得到滿足,未來市場潛力巨大。而公司兩種重組人促紅素產品益比奧和賽博爾銷售額4.62億元,同比增長2.3%,市場份額為41.2%;小分子藥品上半年銷售額增至2.61億元,同比增長3.3%。
在2019年國家醫保目錄調整中,公司多個產品及適應症納入其中:治療多種皮膚疾病的丙酸氟替卡松乳膏(適諾),益賽普用於成人重度斑塊狀銀屑病適應症,益比奧/賽博爾用於非骨髓惡性腫瘤化療引起的貧血適應症,精蛋白鋅重組人胰島素(優泌林)由醫保乙類升至甲類,治療2型糖尿病的百泌達通過談判進入目錄。
2020年6月19日,三生製藥旗下附屬公司三生國健自主研發的注射用伊尼妥單抗(商品名:賽普汀R)正式獲得國家藥品監督管理局(NMPA)批准,獲批的首個適應症為和化療聯合用於治療HER2陽性的轉移性乳腺癌。獲批僅12天後即在全國五省市開出首張處方。7月22日,三生國健正式登陸上海證券交易所科創板。
在研管線加速推進
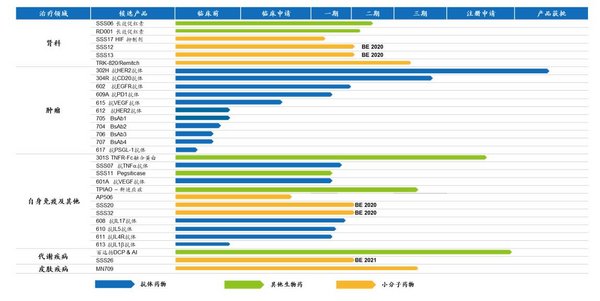
2020上半年,公司繼續立足研發創新,目前擁有32項在研產品,其中22種國家新藥,涵蓋腫瘤科11項、自身免疫性疾病及其他疾病12項。其中預充式益賽普水針劑301S已向國家藥監局申請生產批件並獲受理,公司預計未來3年提交10多個產品的上市申請,以及10-15個新的單抗和雙抗的臨床試驗申請(中美雙報)。
2020上半年公司新增兩項臨床試驗批准,其中611抗IL4Rα抗體獲得FDA臨床試驗批准並獲得NMPA受理,用於治療特應性皮炎;610抗IL5抗體獲得NMPA臨床試驗批准,用於治療重度嗜酸性粒細胞性哮喘。
多項臨床試驗目前進展順利:用於治療多種癌症的抗PD1抗體609A美國I期臨床試驗完成患者入組並開始中國患者入組;用於中重度斑塊狀銀屑病的抗IL-17A抗體608已完成I期臨床試驗者入組並正計劃進行II期臨床試驗;治療血液透析患者瘙癢症的TRK820完成III期臨床橋接試驗第一部分研究;治療貧血的HIF117已開始I期臨床試驗患者入組;治療痛風的SSS11pegitiscase目前正在I期臨床試驗;抗VEGF抗體601A治療AMD的I期臨床患者入組完成,治療DME的I期臨床正在按計劃入組;治療貧血的兩款長效促紅素SSS06和RD001的II期臨床試驗入組順利;TPO治療兒童ITP的III期臨床亦進展順利。
此外,公司還通過對外合作補充在研管線和國際化佈局。2020年伊始,公司作為有限合夥人參與MPM腫瘤創新基金INV,並捐款支持世界領先的癌症研究和治療中心Dana-Farber癌症研究所的早期癌症研究。
極具競爭力的體系化平台優勢
放眼未來,三生製藥將繼續保持集研發、生產、營銷、投資合作為一體的平台優勢,鞏固其在中國生物製藥行業的領先地位,並通過專注開發創新的生物製藥產品,解決未被滿足的醫療需求,造福更多患者。
公司將充分整合多個研發平台超過420人的研發團隊,積極佈局包括單克隆抗體產品、雙特異性抗體、抗體融合蛋白及多個小分子藥物等創新療法,從而為患者帶來多種治療方案。預計今明兩年內將啟動多個III期臨床試驗。
公司擁有約38,000升產能的單克隆抗體設施和哺乳動物細胞、細菌及小分子生產設施,以及在生物醫藥製造領域超過27年的經驗。憑借符合國際質量標準的規模化生產能力,持續向市場提供高質量的生物藥產品。擁有3000逾名專業銷售人員,覆蓋超過2500家三級醫院及超過14000家二級及以下醫院,業務遍及全國。營銷實力近三十年來得到市場驗證和認可,為公司持續增長提供保障。
三生製藥董事長婁競博士表示:「2020年受新冠疫情影響,全球經濟面臨巨大的考驗。我們積極應對挑戰,全力支援疫區,與國家共克時艱,並保持業績的平穩增長,這充分證明了公司研發、生產、銷售和投資合作的體系化競爭優勢。未來,我們將繼續加快在研產品的臨床申請和臨床試驗進程,並進一步擴大生產能力,充分發揮一體化平台的優勢,打造全球領先的中國生物製藥企業,不斷提高創新生物藥的可及性,造福更多患者。」
圖片 - https://photos.prnasia.com/prnh/20200817/2887320-1?lang=2
相關股票: HongKong:1530
- 简体中文 |
- English |
- 日本語 |
- 한국어 |
- Bahasa Indonesia |
- Tiếng Việt